Reverse screening : 신약 개발의 새로운 지평을 여는 접근법


신약 개발의 핵심 중 하나는 특정 화합물이 인체 내에서 어떤 단백질과 결합하여 생리적 효과를 나타내는지를 밝혀내는 것입니다. 이러한 전통적인 신약 개발에서는 단일 단백질 표적에 결합할 수 있는 화합물을 찾아내는 가상 스크리닝 방식이 사용되었습니다.
그러나 역가상 스크리닝(reverse screening)은 특정 화합물이 결합할 수 있는 단백질을 대규모 데이터베이스를 통해 탐색하는 방식으로, 특히 약물 재창출(drug repositioning)과 약물 부작용 예측에 효과적입니다.
역가상 스크리닝의 역할과 가능성
역가상 스크리닝은 새로운 화합물 또는 기존 약물이 예상치 못한 단백질 표적과 결합할 가능성을 찾아내는 방법입니다. 특정 화합물은 여러 단백질과 상호작용하여 다양한 생리적 효과를 나타낼 수 있습니다.
역가상 스크리닝은 여러 단백질을 대상으로 탐색하므로, 이러한 상호작용을 밝혀내는 데 유용합니다. 이 방법은 주로 모양 기반 스크리닝(shape screening), 약리학적 모델 스크리닝(pharmacophore screening), 역도킹(reverse docking)이라는 세 가지 주요 기법을 통해 수행됩니다.
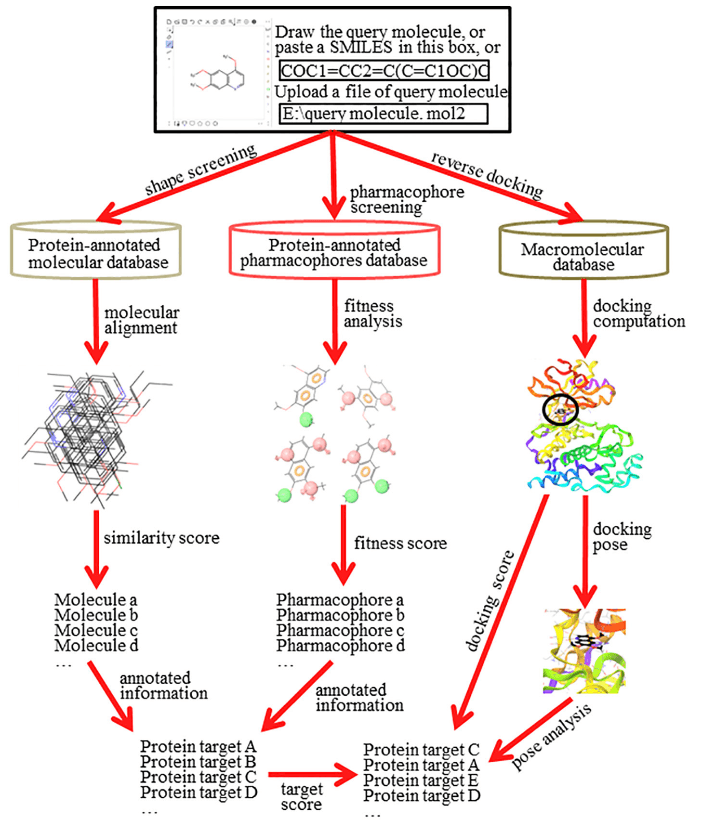
모양 기반 스크리닝(shape screening)
모양 기반 스크리닝은 화합물의 2차원 또는 3차원 구조를, 단백질과 결합하는 다른 화합물들과 비교하여, 구조적으로 유사한 분자는 동일하거나 유사한 단백질과 결합할 수 있다는 가정에 기반해 표적 단백질을 예측하는 방식입니다.
이 방법은 분자들이 공유하는 공통된 모양을 찾아, 해당 모양이 어떤 단백질과 가장 잘 결합할지를 예측합니다.방식이 간단하면서도 매우 빠르고 효율적이며, 특히 분자의 3D 구조가 단백질 결합에 중요한 역할을 할 때 유용합니다. 다만 이 방법은 분자의 작용기나 결합 에너지를 고려하지 않기 때문에, 구체적인 상호작용 예측에는 한계가 있습니다.
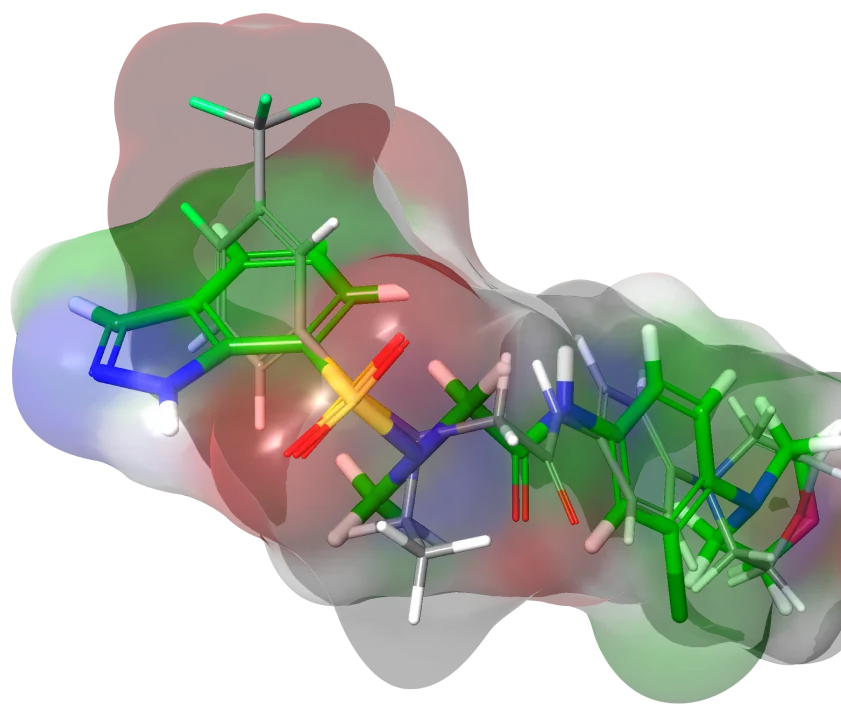
약리학적 모델 스크리닝(pharmacophore screening)
약리학적 모델 스크리닝은 단순한 분자 구조가 아닌, 분자가 가진 작용기를 기반으로 단백질과의 결합을 예측하는 방식입니다. 수소 결합 수용체, 소수성 영역, 전하를 띠는 부분 등, 화합물이 단백질과 상호작용할 때 중요한 역할을 하는 부위(pharmacophore)를 식별하고, 이를 통해 안정적으로 결합할 수 있는 표적 단백질을 예측합니다.
이 방식은 단순히 분자의 모양(shape)만 보는 것이 아니라, 그 안에 포함된 기능적 그룹을 고려하기 때문에 앞서 설명한 모양 기반 스크리닝보다 더 정밀한 결과를 도출할 수 있습니다. 예를 들어, 분자의 크기가 작더라도 중요한 작용기를 다수 포함하고 있다면, 해당 분자는 여러 단백질과 결합할 가능성이 높습니다. 이러한 접근법은 특히 분자의 복잡한 결합 특성을 이해하는 데 유리합니다.
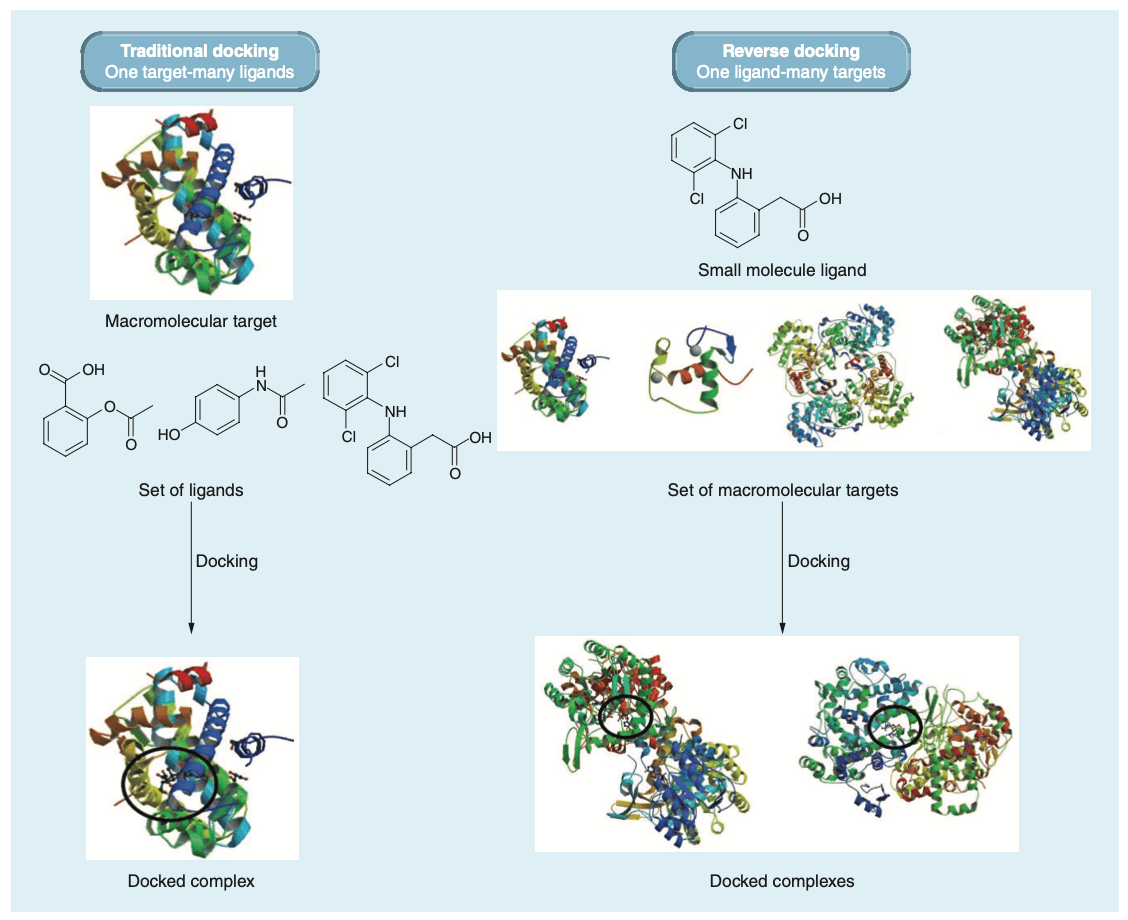
역도킹(reverse docking)
역도킹은 역가상 스크리닝의 세 가지 방식 중 하나로, 가장 정교한 방법에 속합니다. 주어진 화합물이 다양한 단백질의 활성 부위에 결합 가능성을 시뮬레이션하여, 어떤 단백질과 가장 잘 결합하는지를 분석합니다. 이 방법은 기존의 전통적인 도킹 프로그램을 사용해 단백질의 활성 부위에 타겟 분자를 도킹하고, 결합 에너지를 계산하여 가장 낮은 에너지 값을 나타내는 단백질을 잠재적인 표적 단백질로 간주합니다.
역도킹은 매우 정밀한 분석을 제공하지만, 계산 자원을 많이 요구하고 시간이 오래 걸린다는 단점이 있습니다. 그럼에도 불구하고, 단백질과 분자 간의 결합 메커니즘을 정밀하게 예측할 수 있어 약물 표적 탐색에 유용합니다. 또한 다양한 단백질-화합물 결합 구조를 활용함으로써, 단백질의 구조적 유연성까지 고려할 수 있어 복잡한 상호작용을 다룰 때에도 유리합니다.
역가상 스크리닝 응용 사례
역가상 스크리닝의 대표적인 응용 사례로는, 전통 한약재에 포함된 화합물이 어떤 단백질과 결합할 수 있는지를 예측하는 것입니다. 전통 약재의 경우 약리 작용 기전이 명확하지 않은 경우가 많기 때문에, 역가상 스크리닝을 통해 약리 기전을 규명하려는 연구가 활발히 이루어지고 있습니다.
또한 역가상 스크리닝은 약물 재창출(drug repositioning)에도 매우 유용합니다. 약물 재창출이란 이미 개발된 약물을 새로운 질병에 사용할 수 있는 가능성을 찾는 것을 의미합니다.
역가상 스크리닝을 통해 기존 약물이 결합할 수 있는 새로운 단백질 표적을 탐색함으로써, 이를 통해 기존 약물의 예상치 못한 치료 효과를 발견할 수 있습니다.
역가상 스크리닝의 한계와 도전 과제
역가상 스크리닝은 강력한 도구이지만, 여전히 해결해야 할 과제가 많습니다.
첫 번째로, 단백질과 분자 간의 결합을 정확하게 예측하기 위한 스코어링 함수의 정확도에 한계가 있을 수 있습니다. 현재 사용되는 스코어링 함수는 결합 에너지를 평가하는 데 한계가 있어, 실제 생리적 환경에서의 결합 강도를 정확하게 예측하기 어렵습니다.
두 번째는 데이터베이스의 불완전성입니다. 현재 사용되는 많은 단백질 및 화합물 데이터베이스는 모든 단백질 및 화합물 정보를 포괄하지 않으며, 그 크기나 범위에도 한계가 있습니다. 이로 인해 중요한 단백질 표적이 누락되거나, 예측 결과가 제한될 수 있습니다.
세 번째는 단백질의 유연성을 반영한 도킹 방식 구현의 어려움입니다. 대부분의 전통적인 도킹 알고리즘은 단백질을 고정된 구조로 가정하지만, 실제 단백질은 유동적이며 특정 화합물과 결합할 때 구조적 변화를 겪을 수 있습니다. 이러한 유연성을 반영하지 못하는 도킹 방법은 예측 정확도가 낮아질 수 있습니다. (이전 블로그 글 참조, 링크)
AI 기술과 빅데이터를 활용한 역가상 스크리닝의 미래
여러 한계에도 불구하고, 역가상 스크리닝은 앞으로도 발전할 것입니다. AI 및 빅데이터 기반의 새로운 알고리즘이 지속적으로 도입되면, 역가상 스크리닝의 예측 정확도는 더욱 향상될 것으로 기대됩니다. 또한, 데이터베이스가 확장되고 단백질 구조에 대한 정보가 축적됨에 따라, 더 많은 단백질 표적의 탐색이 가능해질 것입니다.