EFMC-ISMC 2024에서 처음 공개된 신약


EFMC-ISMC 2024에서 처음 공개된 신약
2024년 EFMC-ISMC 2024에는 많은 의약화학자분이 참석해 연구 성과에 대한 활발한 공유가 이루어졌습니다. 그중에서도 두 개의 First Disclosure 세션이 많은 주목을 받았는데요, 이 세션에서는 최신 임상 후보 물질의 구조가 처음으로 공개되었습니다. 총 7개 물질로, 각 물질의 특징을 간략히 살펴보겠습니다.
| Name | Target |
|---|---|
| HRX-215 | MKK4 |
| BAY 2413555 | M2 Receptor |
| NVP-EVS459 | Folate receptor |
| GSK484 | PAD4 |
| NVP-DFF332 | HIF-2α |
| CHF-6523 | PI3Kδ |
| AZD-4144 | NLRP3 Inflammasome |
1. Discovery and Development of a First in Class MKK-4 Inhibitor to Increase Liver Regeneration First Disclosure of the Clinical Candidate HRX-215(간부전, 간 이식 환자 대상)
Prof. Stefan LAUFER (UNIVERSITY OF TÜBINGEN, Tübingen, Germany)
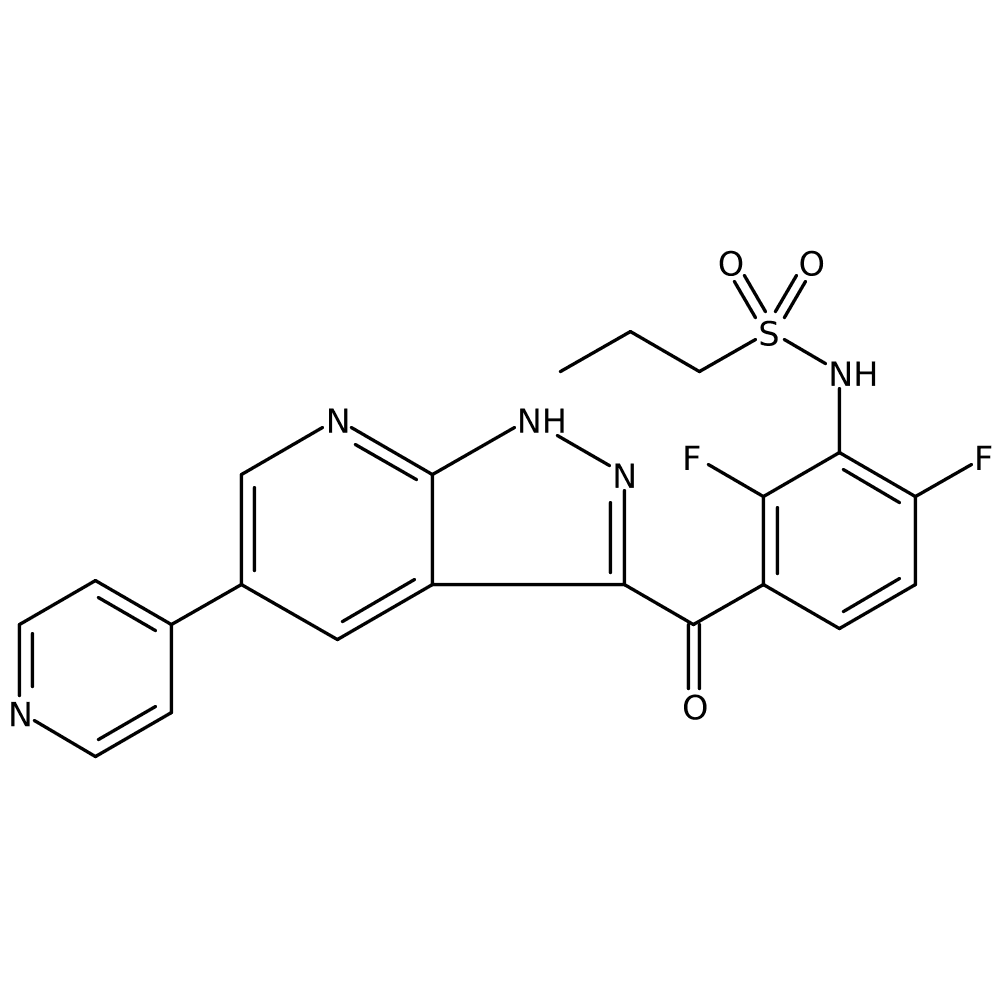
- 이 약물은 간 절제 수술 후 간부전 위험이 높은 환자 또는 간 이식 환자를 돕기 위해 개발되었습니다. MKK4를 억제해 간세포 재생을 촉진하는 ATF2, ELK1 전사 인자를 활성화합니다.
- 쥐와 돼지 모델에서 간 절제 후 간 재생을 증가시켰습니다. 85% 간 절제를 받은 돼지 모델 5마리는 HRX215 투여로 생존했고, 정상적인 행동을 보였으며, 위약군 돼지 모델 6마리 중 5마리는 수술 후 24시간 내에 혼수 상태에 빠져 안락사당했습니다.
- 2022년 5월에 완료된 1상 임상시험 결과, 인간에게 안전하고 우수한 약동학적 특성을 보여 현재 2상을 계획 중입니다.
*출처: https://www.cell.com/cell/fulltext/S0092-8674(24)00225-3
2. Discovery of BAY 2413555, First Highly Selective Positive Allosteric Modulator of the M2 Receptor to Restore Autonomic Balance in Heart Failure Patients(심부전 환자의 자율신경 회복)
Dr Alexandros VAKALOPOULOS (BAYER, Wuppertal, Germany)
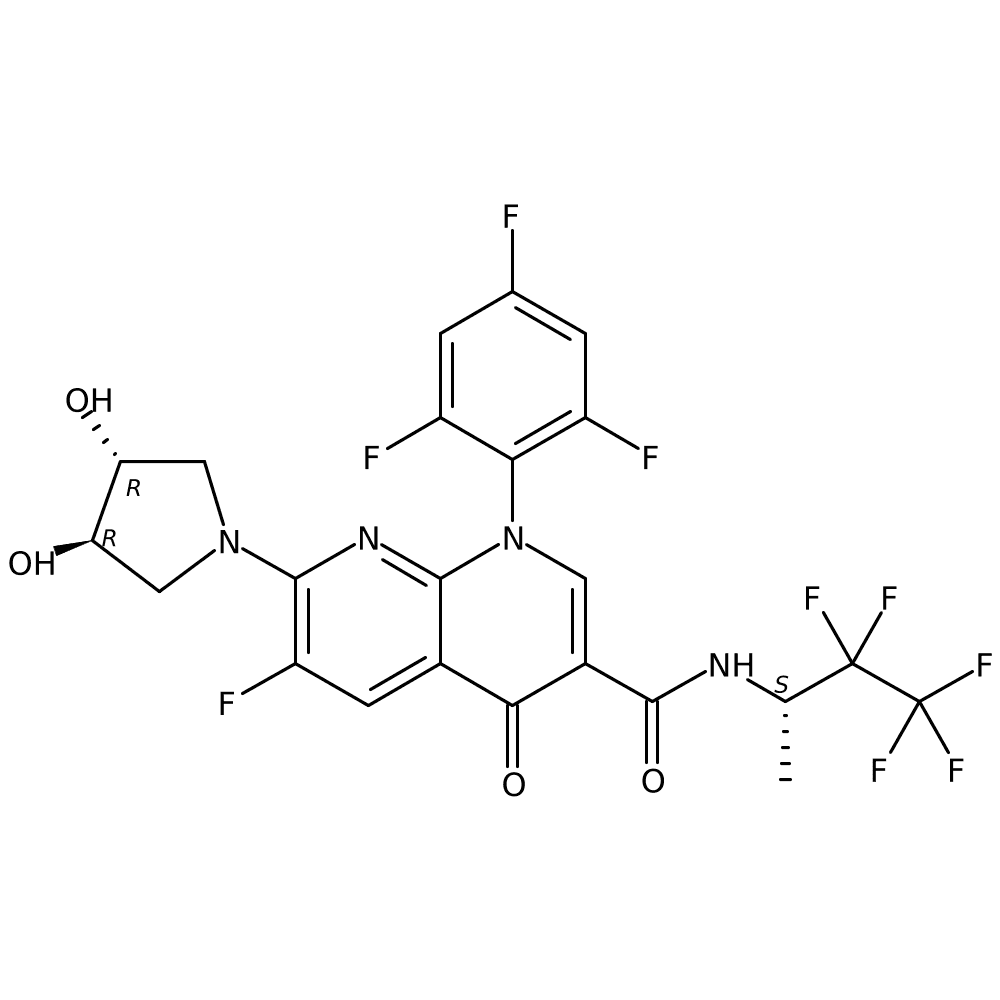
- 심부전 환자의 자율신경 균형을 회복하기 위해 개발되었습니다.
- M2 수용체를 통해 심박수를 조절하고, 교감신경을 억제하며 부교감신경을 활성화해 자율신경의 균형을 회복하는 데 도움을 줍니다.
- 2023년 3월에 1상이 종료되었으며, 추가 2상 계획에 대한 발표는 없었습니다.
*출처: https://clinicaltrials.bayer.com/study/20623/
3. Discovery of NVP-EVS459, a Low Molecular Weight Folate Receptor Targeting Radioconjugate for the Treatment of Folate Receptor Positive Cancers with First-In-Class Potential(선택적 암세포 파괴)
Dr Philipp HOLZER (NOVARTIS PHARMA AG, Basel, Switzerland)
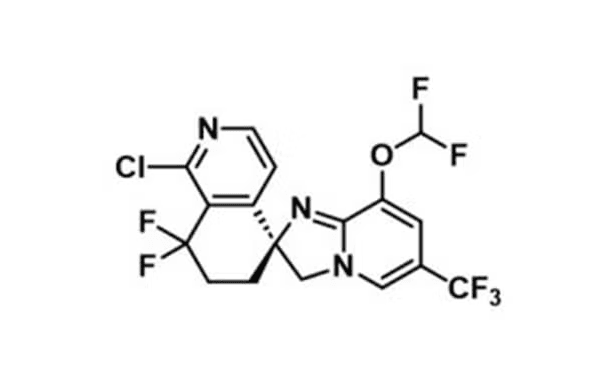
-
Folate Receptor가 많이 발현되는 난소암, 비소세포폐암 등의 암 치료에 유망한 약물입니다.
-
암세포는 빠른 증식을 위해 FR을 과다 발현해 엽산을 흡수하는 데, EVS459 물질에 방사성 동위원소 루테튬-177을 결합함으로써 방사선을 암세포에 직접 전달하여 선택적으로 파괴합니다.
- 2024년 9월 6일에 임상 1상이 개시되었습니다.
*출처: https://www.careacross.com/clinical-trials/trial/NCT06376253
4. Discovery of Clinical Candidate GSK484: a Novel "Irresistible" Chemical Class for the Treatment of Malaria(말라리아)
Dr Jorge FERNANDEZ (GSK, Tres Cantos, Spain)
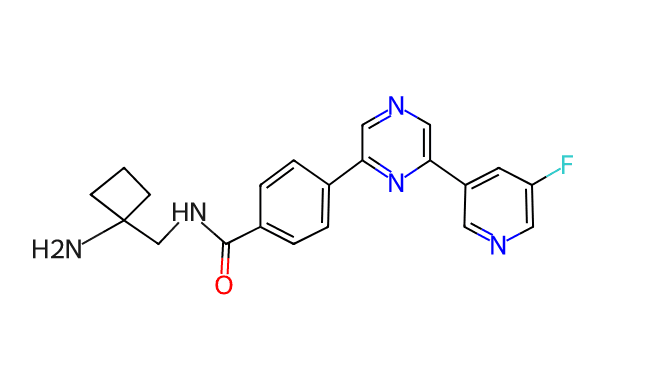
- Peptidylarginine deiminase 4는 칼슘 의존성 효소로, 칼슘이 없을 때는 IC50 값이 50nM, 칼슘 2mM 환경에서는 250nM으로 측정됩니다.
- PAD4는 염증 반응에 중요한 효소로, 아르기닌을 시트룰린으로 변환하는 ‘시트룰린화’ 반응을 촉매합니다.
- 이 과정은 염증 반응, 면역 반응 조절, 중성구 세포외 덫(neutrophil extracellular traps) 형성에 중요한 역할을 하며, PAD4 저해는 말라리아 감염 시 발생하는 과도한 염증 반응을 줄여 치료에 도움을 줄 수 있습니다.
*출처: https://academic.oup.com/jleukbio/article/111/6/1235/6885198
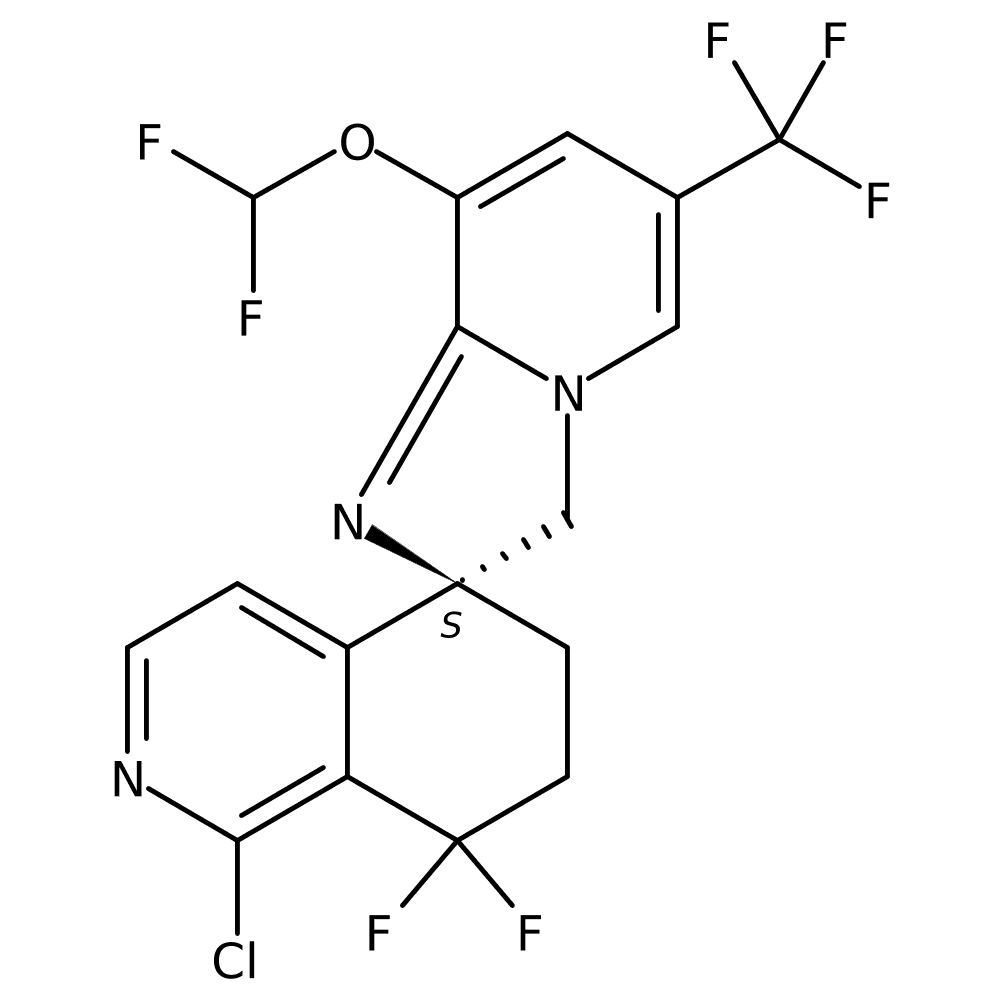
5. Discovery of NVP-DFF332 as a Selective Inhibitor of the Transcription Factor Hypoxia-Inducible Factor-2ALPHA (HIF-2α)(암 세포 성장 저하)
Dr Robin FAIRHURST (NOVARTIS, Basel, Switzerland)
-
HIF-2α를 억제하는 경구용 저분자 화합물은 clear cell renal cell carcinoma(ccRCC)를 대상으로 개발되고 있습니다. HIF-2α는 저산소 환경에서 암세포의 성장을 촉진하는 중요한 단백질로, ccRCC에서 높은 발현을 보입니다.
-
임상 1상에서 Disease Control Rate(DCR)은 52.5%로, 환자의 절반 이상에서 암이 진행되지 않거나 크기가 줄어드는 반응을 보였습니다.
-
하지만 최적 용량을 결정하기 전에 사업적 결정으로 인해 중단된 한계가 있습니다.
*출처: https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.4513
6. First-time Disclosure of Clinical Candidate CHF-6523, an Inhaled Selective PI3Kδ Inhibitor for the Treatment of Chronic Obstructive Pulmonary Disease(염증성 사이토카인)
Dr Paolo BRUNO (CHIESI FARMACEUTICI SPA, Parma, Italy)
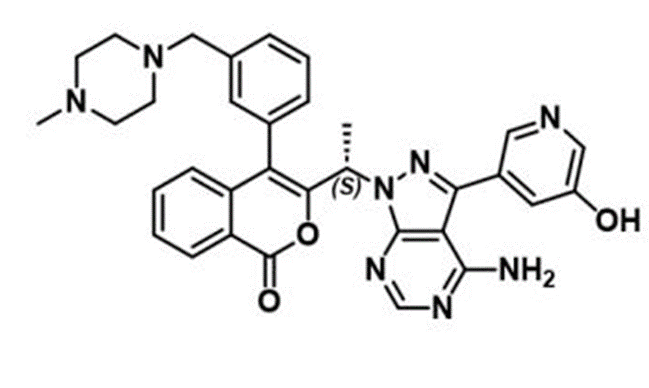
- 흡입용 건조 분말 제형으로 제공됩니다.
- IL-6와 같은 염증성 사이토카인을 혈장과 가래에서 측정하였으며, 이를 바탕으로 치료 전후의 변화를 평가하였습니다.
- 2022년 12월에 임상 1상이 완료되었으며, 2상 임상시험 계획은 아직 발표되지 않았습니다.
7. Inhibition of the NLRP3 Inflammasome is a Promising Concept to Treat a Variety of Inflammatory Diseases: AZD-4144(염증성, 심혈관 질환)
Dr Anders JOHANSSON (ASTRAZENECA, Molndal, Sweden)
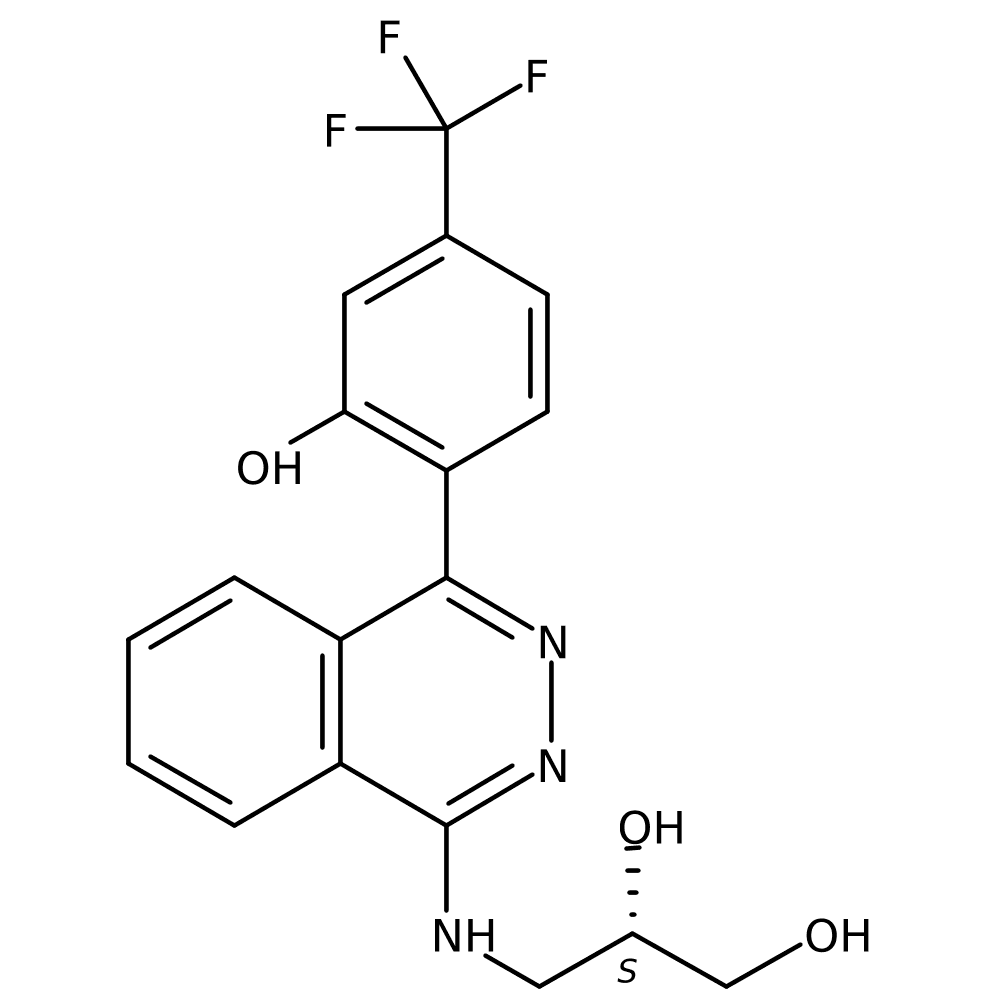
- NLRP3 인플라마좀은 세포 내에서 IL-1β, IL-18 등의 염증성 사이토카인을 활성화하여 염증 반응을 유도하는 중요한 단백질 복합체입니다.
- 이 인플라마좀의 과도한 활성화는 다양한 만성 염증성 질환에서 관찰되며, 현재 AZD-4144는 염증성 및 심혈관 질환 치료를 목표로 개발 중입니다.
- 임상 1상이 진행 중이며, 2025년에 완료될 예정입니다.
*출처: https://www.astrazenecaclinicaltrials.com/study/D9440C00001/