2024년 블록버스터 약물 TOP10


2024년 block buster 약물
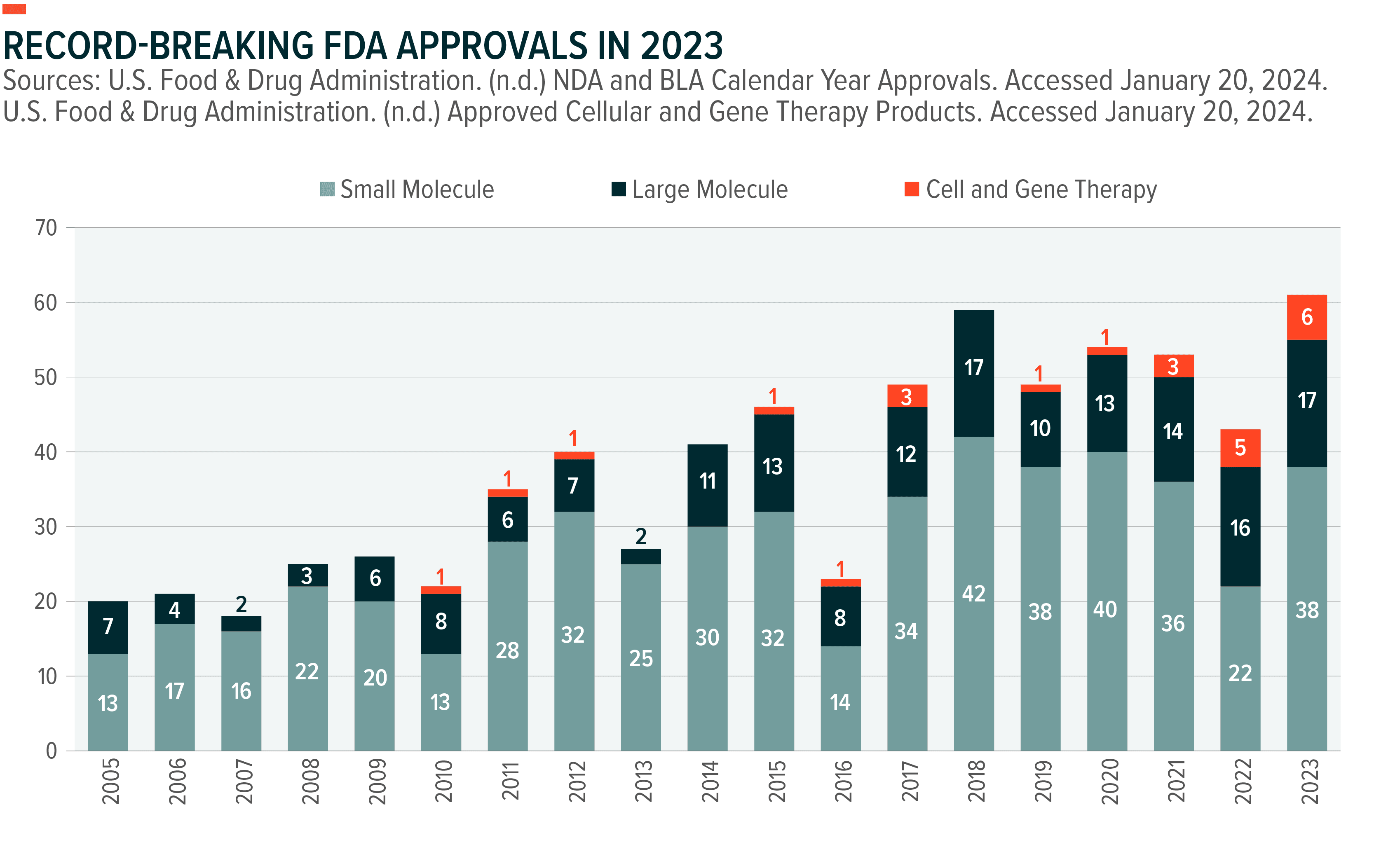 FDA에서 작년에는 55개의 신약을 승인했었는데요, 올해 상반기에는 21개의 약물이 승인되었습니다. 작년에는 2023년도 승인 약물에 대해 소개해드렸는데요. 이번에는 Evaluate에서 선정한 올해 승인되는 잠재 매출이 가장 기대되는 약물 10가지에 대해서 다뤄보도록 하겠습니다.
FDA에서 작년에는 55개의 신약을 승인했었는데요, 올해 상반기에는 21개의 약물이 승인되었습니다. 작년에는 2023년도 승인 약물에 대해 소개해드렸는데요. 이번에는 Evaluate에서 선정한 올해 승인되는 잠재 매출이 가장 기대되는 약물 10가지에 대해서 다뤄보도록 하겠습니다.
| Drug name | Active Ingredient | Company | Target/Modality | Disease | Approval Date |
| Zelsuvmi | berdazimer | Ligand Pharmaceuticals | NO-releasing agent | molluscum contagiosum | 01월 05일 |
| Exblifep | cefepime, Enmetazobactam | Allecra Therapeutics | Cephalosporin and β-lactamase inhibitor | complicated urinary tract infections | 02월 22일 |
| Letybo | letibotulinumtoxinA-wlbg | Hugel | nAChR antagonist; SNAP25 inhibitor | temporarily improve the appearance of moderate-to-severe glabellar lines | 02월 29일 |
| Tevimbra | tislelizumab-jsgr | BeiGene | PD1-targeted mAb | unresectable or metastatic esophageal squamous cell carcinoma | 03월 13일 |
| Rezdiffra | Resmetirom | Madrigal Pharmaceuticals | TRβ agonist | noncirrhotic non-alcoholic steatohepatitis with moderate to advanced liver scarring | 03월 14일 |
| Tryvio | Aprocitentan | Idorsia | ETA/ETB receptor antagonist | hypertension | 03월 19일 |
| Duvyzat | Givinostat | Italfarmaco | HDAC inhibitor | Duchenne muscular dystrophy in individuals aged 6 years and older | 03월 21일 |
| Winrevair | sotatercept-csrk | Merck & Co. | ACTRIIA–Fc fusion protein | pulmonary arterial hypertension | 03월 26일 |
| Vafseo | Vadadustat | Akebia Therapeutics | HIF-PH inhibitor | anemia due to chronic kidney disease | 03월 27일 |
| Voydeya | Danicopan | AstraZeneca | Factor D inhibitor | extravascular hemolysis with paroxysmal nocturnal hemoglobinuria | 03월 29일 |
| Zevtera | ceftobiprole medocaril Sodium | Basilea Pharmaceutica Ltd. | Penicillin-Binding Proteins | certain bloodstream infections, bacterial skin and associated tissue infections, and community-acquired bacterial pneumonia | 04월 03일 |
| Lumisight | Pegulicianine | Lumicell, Inc. | 유방암 조직 식별 형광인자 | To use as an optical imaging agent for the detection of cancerous tissue | 04월 17일 |
| Anktiva | nogapendekin alfa inbakicept-pmln | ImmunityBio, Inc. | IL-15 receptor | bladder cancer | 04월 22일 |
| Ojemda | Tovorafenib | Day One Biopharmaceuticals, Inc. | BRAF V600E | relapsed or refractory pediatric low-grade glioma | 04월 23일 |
| Xolremdi | Mavorixafor | X4 Pharmaceuticals | CXCR4 | WHIM syndrome (warts, hypogammaglobulinemia, infections and myelokathexis) | 04월 26일 |
| Imdelltra | tarlatamab-dlle | Amgen Inc. | DLL3 | extensive stage small cell lung cancer | 05월 16일 |
| Rytelo | Imetelstat | Geron Corporation | Telomerase | low- to intermediate-1 risk myelodysplastic syndromes | 06월 06일 |
| Iqirvo | elafibranor | GENFIT, Ipsen | PPARα/δ | Primary biliary cholangitis | 06월 10일 |
| Sofdra | Sofpironium | Botanix Pharmaceuticals | Acetylcholine receptors | Primary axillary hyperhidrosis | 06월 20일 |
| Piasky | crovalimab-akkz | Roche | Complement C5 | Paroxysmal nocturnal hemoglobinuria | 06월 20일 |
| Ohtuvayre | Ensifentrine | Verona Pharma | Dual phosphodiesterase 3/4 | Chronic obstructive pulmonary disease | 06월 26일 |
| Kisunla | donanemab-azbt | Eli Lilly | Amyloid plaque | Alzheimer’s disease | 07월 02일 |
주요 사항
- Eli Lilly는 알츠하이머병 치료제 Donanemab의 승인으로 CNS 파이프라인 확장에 성공했습니다.
- Moderna는 COVID-19 백신 외에도, 획기적인 mRNA 기술을 활용해 호흡기세포융합바이러스(RSV) 백신인 mRNA-1345의 승인을 기대하고 있습니다.
- Bristol Myers Squibb은 과거에 인수한 Karuna Therapeutics를 통해 정신분열증 치료제 KarXT로 신경과학 파이프라인을 확장하고 있습니다.
1. KarXT(xanomeline-trospium)- 알츠하이머
▶ Company: Bristol Myers Squibb/Karuna Therapeutics
▶ Indication: Psychiatric and neurological conditions
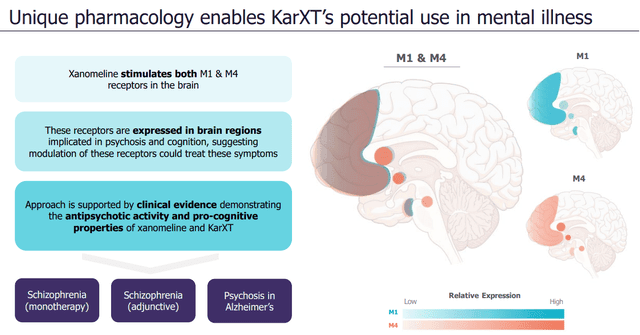
KarXT는 xanomeline과 trospium 두 약물을 병용 투여합니다. 이는 수십 년 만에 처음으로 정신분열증 치료에 새로운 메커니즘으로 접근한 약물로, xanomeline은 M1/M4 무스카린 콜린성 수용체 작용제로서 도파민이나 세로토닌 수용체를 직접적으로 차단하는 데만 의존하는 현재 치료 방법과 다르다는 점에 의의가 있습니다. 이러한 새로운 접근법은 추체외로 증상, 즉 파킨슨병의 몸 떨림 증상과 같은 부작용을 수반하지 않아 더욱 유망한 치료제로 주목받고 있습니다.
M1 수용체는 대뇌피질에 분포하고 있으며, M1 수용체의 활성화는 인지 기능 개선 및 학습 능력 향상에 도움이 됩니다. M4 수용체는 보상 체계에 관여하는 선조체에 분포하고 있으며, M4 수용체의 활성화는 도파민 신호 전달 조절을 통해 환청 등의 양성 증상을 완화합니다.
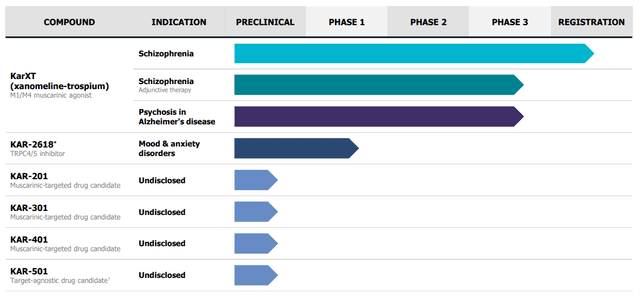
KarXT는 알츠하이머병과 양극성 장애에 대한 잠재적 치료제로 가능성을 테스트하고 있으며, 최종 결정일(PDUFA)은 9월 26일입니다.
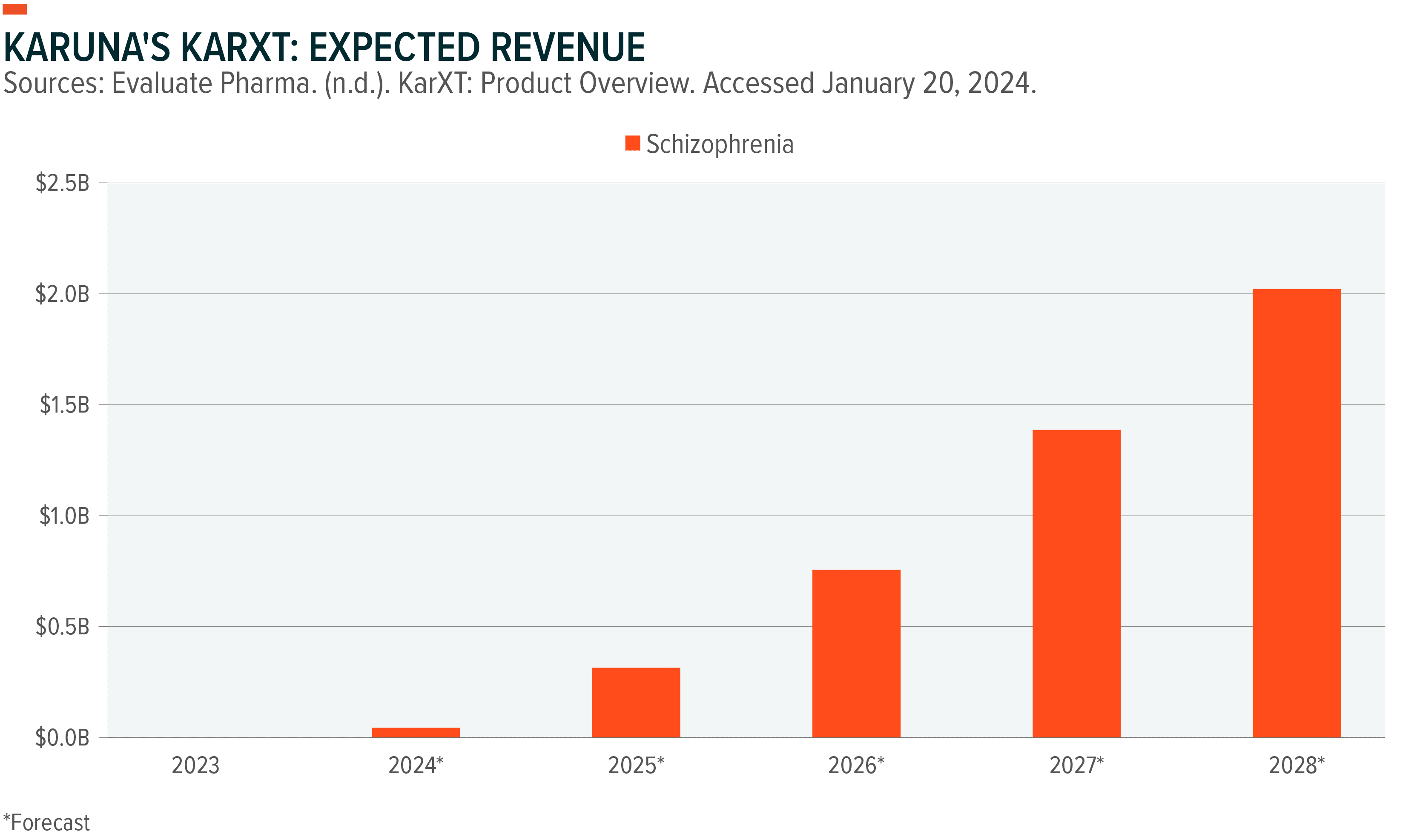
Karuna Therapeutics는 최근 140억 달러에 BMS에 인수된 회사입니다. 정신분열증 치료제 KarXT는 2028년에 20억 달러의 매출을 달성할 것으로 예상되며, 최대 매출은 60억 달러에 이를 것으로 보입니다.
2. Donanemab - 알츠하이머
▶ Company: Eli Lilly
▶ Indication: Alzheimer's disease
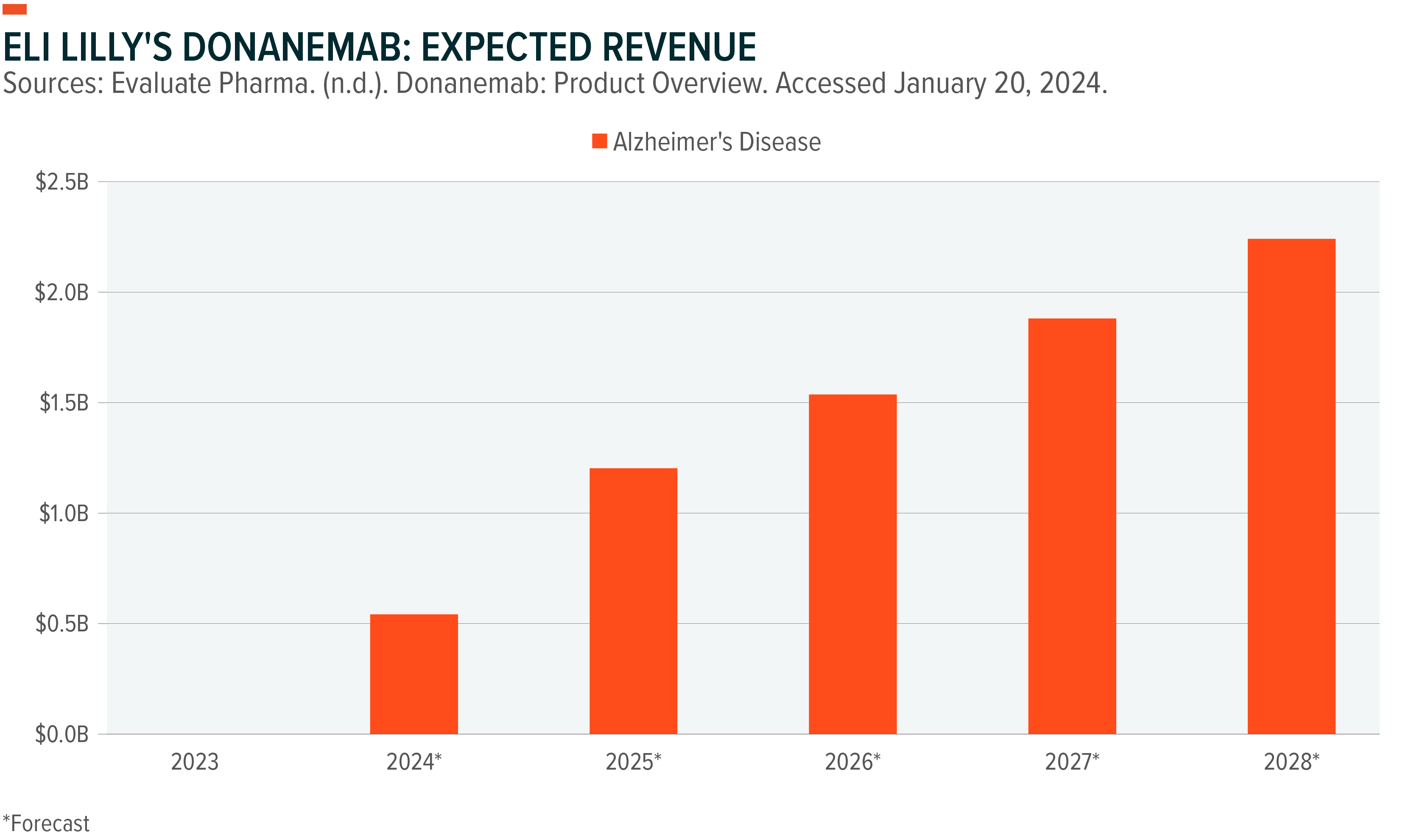
현재 미국에서는 600만 명의 성인이 알츠하이머를 앓고 있습니다. 2050년까지는 1,300만 명까지 증가할 것으로 예상되고 있는데요, 따라서 이번 승인으로 Eli Lilly의 신경 관련 매출은 2028년까지 연평균 18%의 CAGR을 기록할 것으로 예상됩니다.
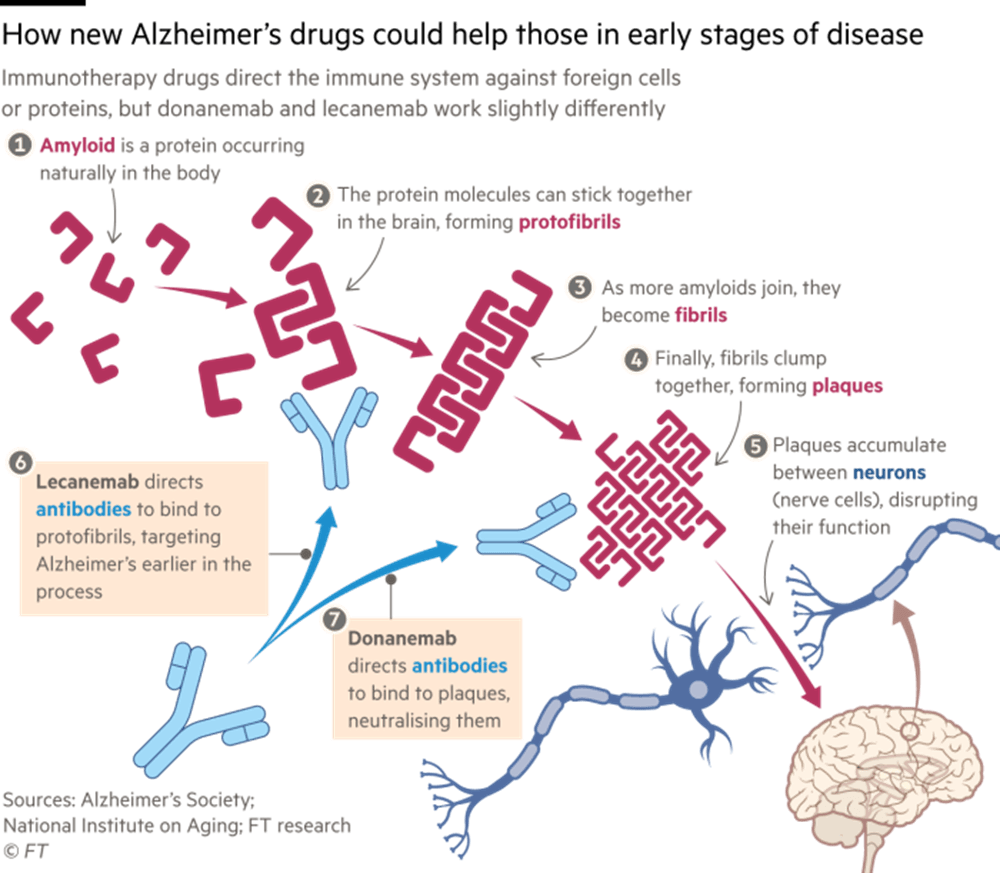
Donanemab과 2023년에 승인된 Leqembi는 항체라는 점에서는 같지만, 아밀로이드 플라크 형성 과정에서 어느 단계에 개입하는지에 차이를 보입니다. 위 그림과 같이 Donanemab은 fibrils에서 plaques로 형성되는 과정을 막고, Leqembi는 protofibrils에서 fibrils로 전환되는 과정을 막습니다.
약효에서도 차이를 보이는데요, Donanemab은 임상 3상에서 평균 84%의 아밀로이드 플라크 감소를 보여주었고, 위약 환자는 1% 감소에 그쳤습니다. 이는 인지 기능 저하 또한 35% 늦춘 것으로, Leqembi가 인지 저하를 27% 늦추었다는 점을 감안했을 때 매우 고무적입니다.
Eli Lilly는 최근 Roche와의 협력을 통해 혈액 검사를 통한 새로운 진단 방법을 개발하고 있습니다. 알츠하이머는 증상 발현 후 평균 2.8년이 지나서야 진단을 받는 경우가 많아, 적절한 시기에 치료가 어렵고 조기 발견의 필요성이 강조되고 있습니다. 이런 연구적 시도를 통해 Eli Lilly는 계속해서 알츠하이머 치료제 시장을 선도하고 있습니다.
3. Resmetirom - 지방간염
▶ Company: Madrigal Pharmaceuticals
▶ Indication: Nonalcoholic steatohepatitis (NASH)
2028년 예상 매출액 21억 달러의 마드리갈 파마슈티컬스(Madrigal Pharmaceuticals)의 Resmetirom은 THR-β 작용제입니다. 현재 FDA에서 비알코올성 지방간염(NASH) 치료제로 승인을 받았으며, NASH 유병률이 전체 성인 인구의 6.5%에 달할 것으로 보여 그 가치가 높게 평가되었습니다.
Resmetirom은 이전 블로그에서 다루었어서, 해당 글을 참고 부탁드립니다.
첫 NASH(MASH) 치료제 '레즈디프라' FDA 승인 : 신흥 블록버스터 약물의 등장 (hits.ai)
4. Sotatercept - 고혈압
▶ Company: Merck
▶ Indication: Pulmonary Arterial Hypertension (PAH)
2023년에 블록버스터로 예상되었던 머크의 폐동맥 고혈압(PAH) 치료제 sotatercept가 승인되었습니다. 폐동맥 고혈압은 폐의 동맥이 좁아지고 혈압이 비정상적으로 상승하는 질환으로, 치료하지 않으면 심부전으로 이어질 수 있습니다. Evaluate는 2028년까지의 매출액을 약 20억 달러로 예상했다가, 이를 두 배로 상향 조정했습니다. 이 약은 115억 달러에 달하는 Acceleron Pharma 인수의 결과물이었습니다.
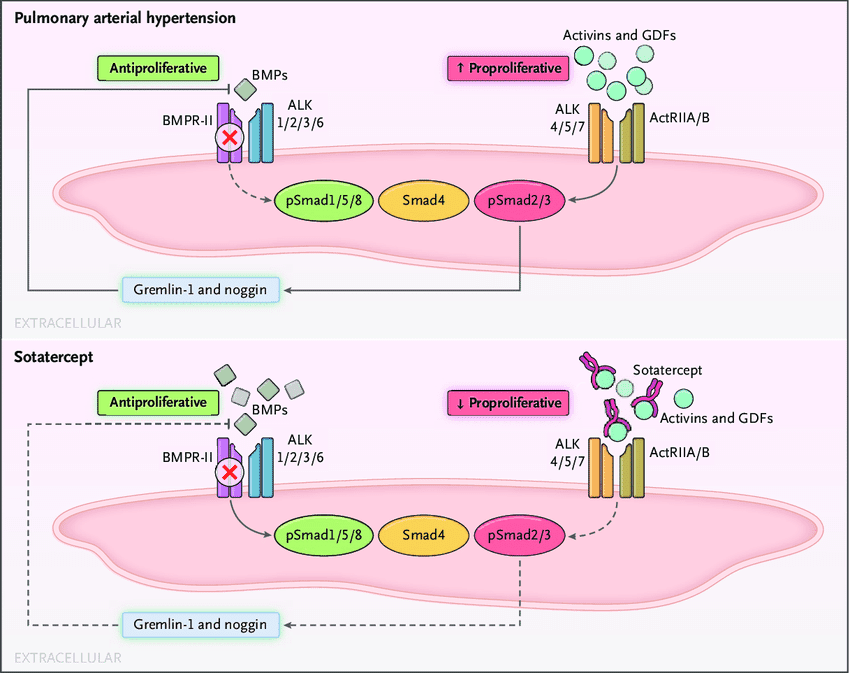
기존 치료제들이 혈관을 확장시키거나 폐혈관 저항을 줄이는 방식으로 작용하는 데 반해, sotatercept는 액티빈 수용체 IIA-Fc 융합 단백질에 작용해 질병을 유발하는 근본적인 단백질에 보다 직접적으로 작용하며, 혈관 리모델링을 조절하는 새로운 기전을 갖고 있습니다.
혈관 세포 증식(proliferation)을 촉진하는 신호와 항증식(anti-proliferation) 신호 경로 사이의 균형을 조절합니다.
액티빈 수용체는 혈관의 비정상적인 성장과 리모델링에 중요한 역할을 하는데, 이를 억제함으로써 혈관 증식이 감소하고 혈관 벽이 얇아져 혈류 역학을 개선하는 데 도움이 됩니다.
5. Datopotamab deruxtecan
▶ Company: Daiichi Sankyo & AstraZeneca
▶ Indication: Lung & Breast Cancer
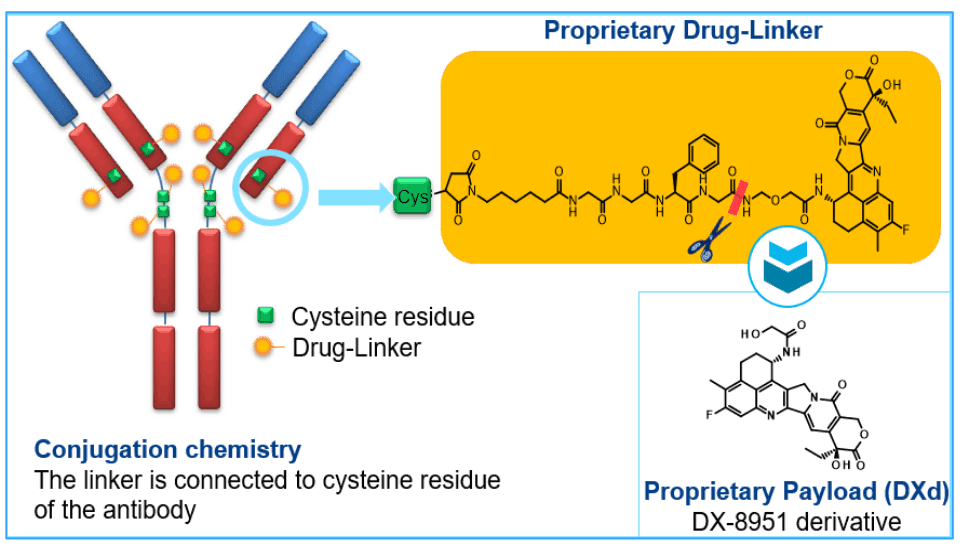
Datopotamab deruxtecan은 Tumor-associated calcium signal transducer 2(TROP2)라는 세포 표면 단백질을 표적하는 항체-약물 접합체(ADC)입니다. 적응증은 비소세포폐암(NSCLC)과 삼중음성유방암(TNBC) 등 다양한 상피성 종양이며, 2차 치료제로 개발되었습니다. 올해 2월에 승인 신청이 이루어졌고, 4월에 허가 심사가 시작되었습니다.
원래는 유전자형이나 조직 하위 유형과 상관없이 전체 NSCLC 환자를 대상으로 2차 치료제를 개발하고 있었습니다. 하지만 임상 3상 과정에서 환자 하위 그룹 분석을 실시한 결과, non-squamous NSCLC 환자에게만 약효를 보여 환자 범위를 축소해 허가를 추진하게 되었습니다.
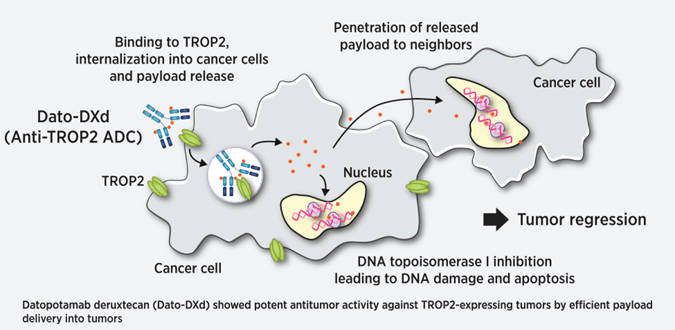
약물의 작용 원리는 다음과 같습니다. Dato-DXd는 암세포 표면의 TROP2에 결합해 복합체를 형성합니다. 이 복합체는 종양 세포 내부로 흡수되어 리소좀에서 분해됩니다.
이 단계에서 Dato-DXd의 각 구성요소가 분리되며, 이후 DXd가 세포질로 방출되어 세포핵으로 이동합니다.
DXd는 세포핵에서 Topoisomerase I을 억제해 DNA 복제를 방해하고, DNA 손상을 유발합니다. 결과적으로 종양 세포의 사멸을 유도하며, 정상 세포는 공격하지 않고 암세포에 특이적으로 작용합니다.
6. Acoramidis - 심근병증
▶ Company: BridgeBio Pharma
▶ Indication: ATTR-CM
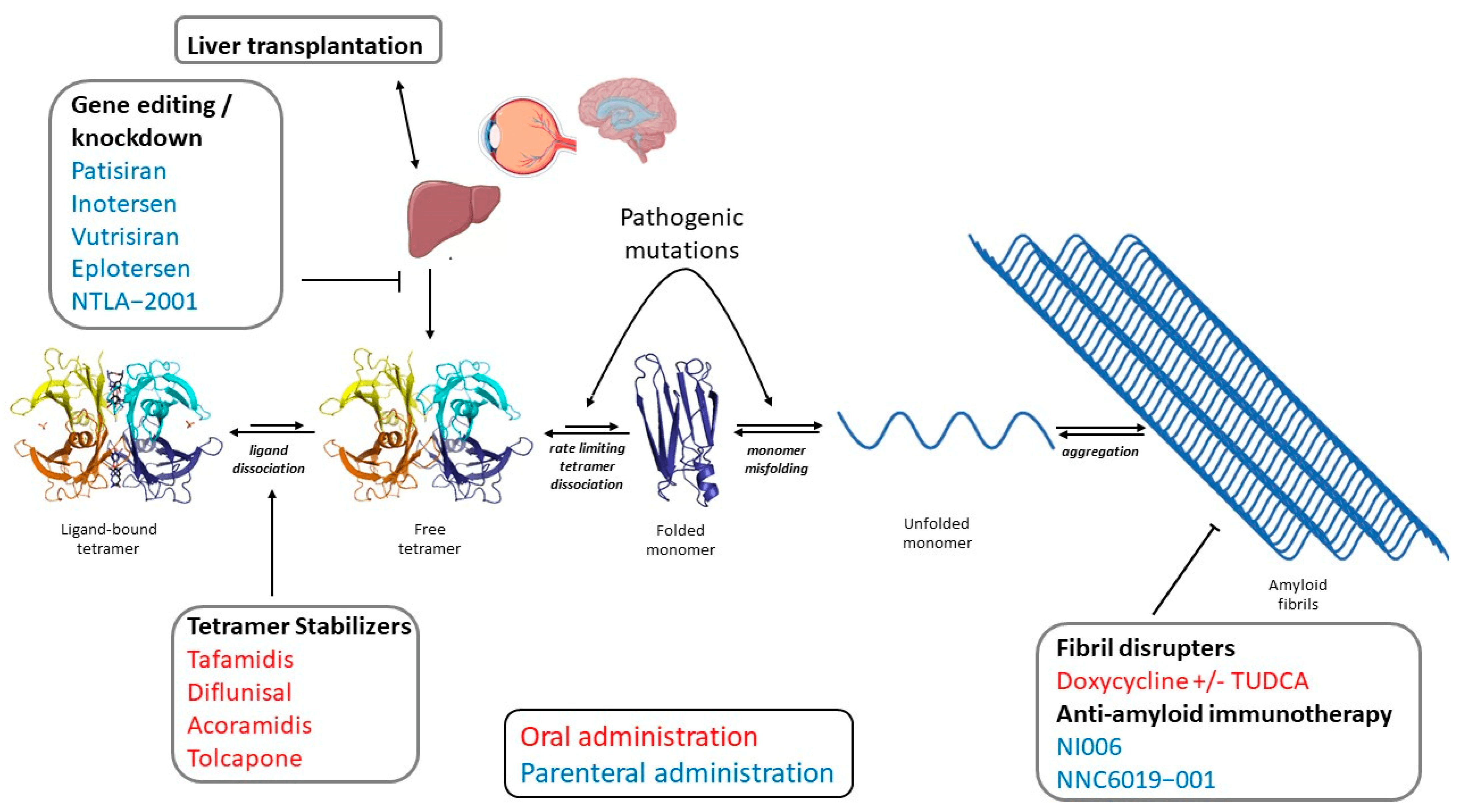
Transthyretin(TTR) stabilizer 계열의 경구용 약물인 이 약물은 현재 FDA에서 검토 중입니다. BridgeBio는 지난해 말, 심장 질환인 트랜스티레틴 아밀로이드 심근병증(ATTR-CM) 치료제 Acoramidis의 임상 결과를 바탕으로 주가를 400% 이상 끌어올리기도 했습니다. 임상 3상 시험에서 위약 대비 심혈관 관련 사망률을 30% 감소시킨 점이 주목을 받았는데요, 현재는 화이자의 기존 약물 Tafamidis와 시장에서 경쟁할 것으로 보입니다.
이 약물의 작용 기전은 다음과 같습니다. 먼저, TTR 단백질의 테트라머 형태를 안정화시키는 저분자 화합물입니다. TTR 단백질이 분해되면 독성 단백질 섬유(amyloid fibrils)로 전환되어 심장 등 다른 장기에 축적되는데, 이 과정을 방지하는 것입니다.
7. mRNA-1345
▶ Company: Moderna
▶ Indication: Pre-Registration for Respiratory Syncytial Virus (RSV) Infections
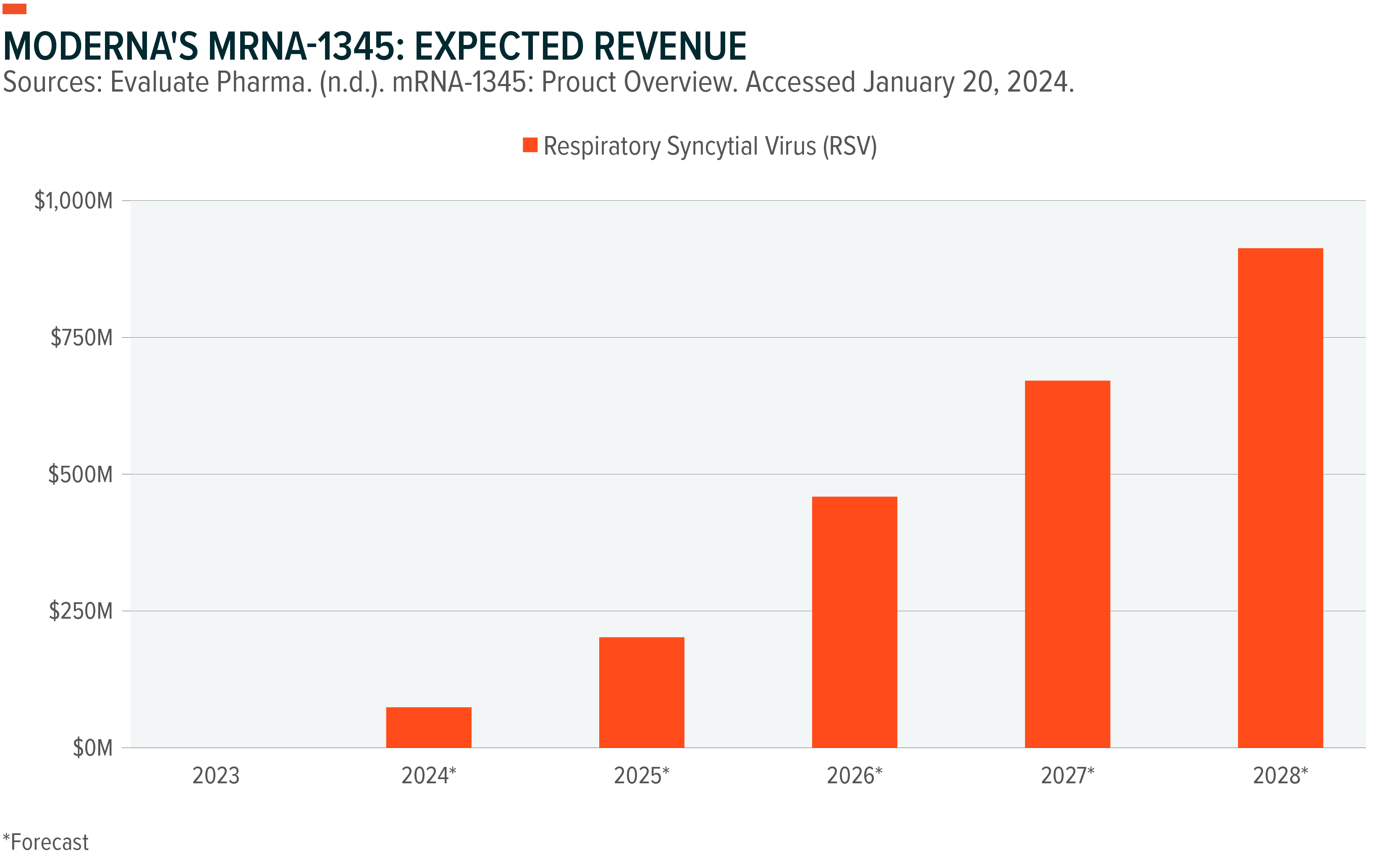
모더나는 COVID-19 백신 Spikevax로 458억 달러를 벌어들이며 mRNA 백신에 대한 연구를 지속해왔는데요, 이번에는 호흡기세포융합바이러스(RSV) 백신인 mRNA-1345가 올해 FDA 승인을 받을 것으로 예상됩니다. RSV는 일반인에게는 감기처럼 느껴지지만, 영유아와 노인에게는 위험하게 작용하는 질환입니다. RSV 시장은 2030년까지 100억 달러 이상으로 성장할 것으로 예상됩니다.
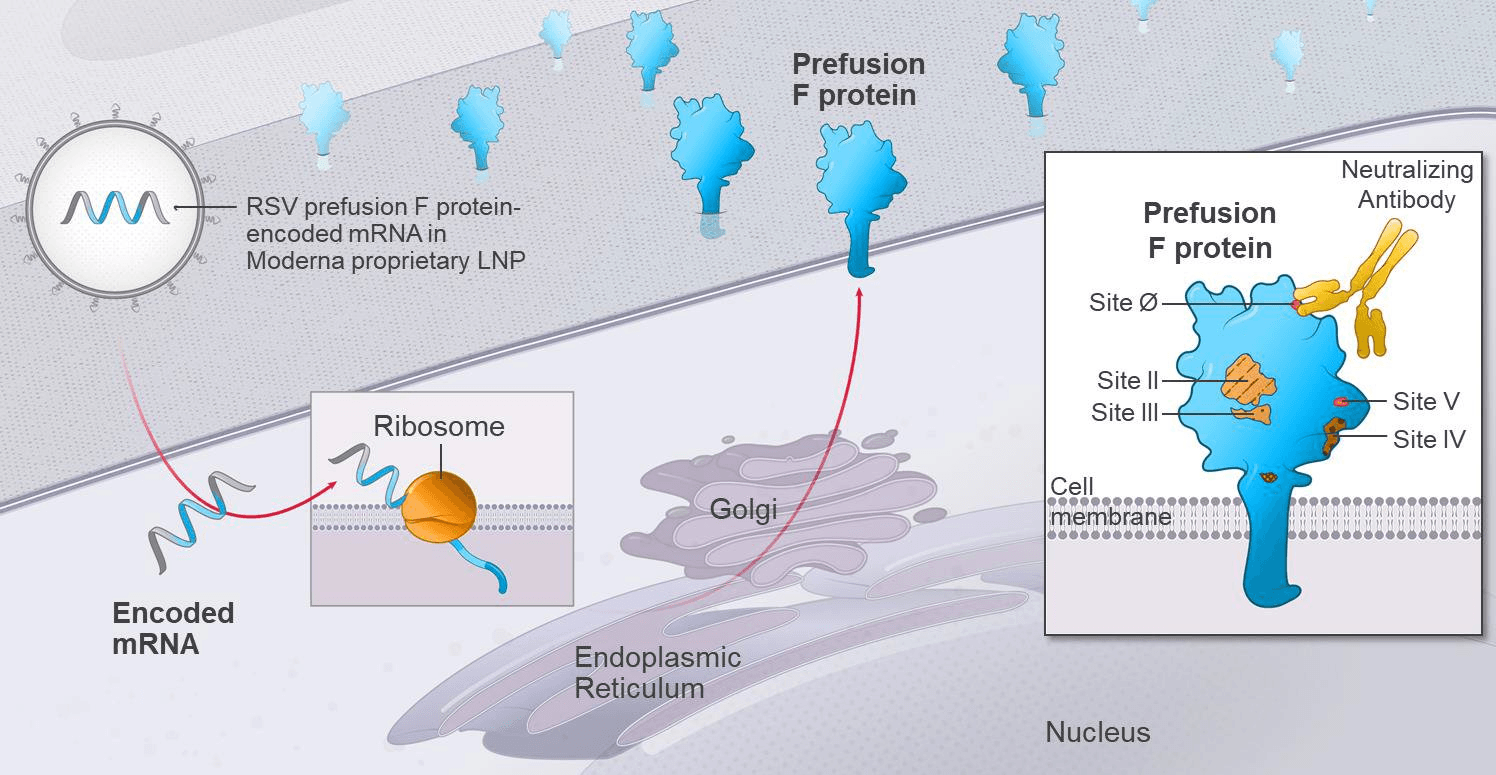
mRNA-1345는 RSV의 F 단백질을 암호화하는 mRNA를 포함하며, 이 mRNA는 세포 내에서 단백질 합성을 유도해 RSV F 단백질을 생성합니다. F 단백질은 RSV가 숙주 세포에 부착하고 침투하는 데 필요한 단백질로, 바이러스의 RNA가 숙주 세포 안으로 들어올 수 있도록 합니다.
이 단백질은 숙주 세포에 융합되기 전(prefusion)과 융합된 후에 따라 구조가 달라지며, mRNA-1345는 prefusion F 단백질을 저해함으로써 바이러스가 RNA를 세포 안으로 주입하기 전에 차단해 약효를 극대화합니다.
생성된 RSV 단백질은 체내 면역 시스템에 의해 외래 항원으로 인식됩니다. 이에 따라 면역 시스템은 항체를 생성하고, T세포 반응을 통해 RSV를 효과적으로 공격할 준비를 합니다. 이 과정을 통해 RSV에 노출되었을 때 신속하고 강력한 면역 반응이 발생해 감염을 예방하거나, 감염되더라도 중증도를 낮출 수 있는 방식으로 체내에서 작용하게 됩니다.
작년 5월에 최초의 RSV 백신으로 승인된 GSK의 Arexvy와 8월에 승인된 Abrysvo는 모두 mRNA 기술을 사용하지 않았다는 점에서 mRNA 기반 경쟁 약물과 차별화됩니다. 뿐만 아니라, ConquerRSV 시험에서 mRNA-1345는 RSV에 대해 83.7%의 예방 효과를 보여 Arexvy(82.6%)와 Abrysvo(61.1%)보다 우위를 점하고 있습니다.
8. Anktiva (N-803) - 비근육 침윤성 방광암
▶ Company: ImmunityBio
▶ Indication: BCG-unresponsive non-muscle-invasive bladder cancer (NMIBC) carcinoma in situ (CIS)

Anktiva는 BCG(칼메트–게랭 간균) 치료에 반응하지 않는 비근육침윤성 방광암(NMIBC) 치료를 위한 면역 치료제입니다. 이 약물은 IL-15 수용체 작용제 역할을 하여 면역 시스템을 활성화하고, 암세포와 싸우도록 돕습니다.
Anktiva는 항체와 사이토카인이 융합된 superagonist입니다. 이 조합은 NK 세포와 CD8⁺ T 세포를 활성화해 암세포를 효과적으로 공격하고 파괴할 수 있도록 합니다. 이를 통해 체내 면역 시스템이 암세포를 인식하고 공격하는 능력을 크게 향상시킵니다.
Anktiva와 Bacillus Calmette–Guérin(BCG) 백신을 방광 내에 병용 투여했을 때, 치료받은 환자 중 62%가 완전 반응(CR)을 보였으며, 이 중 40%는 24개월 이상 약효가 유지돼 임상적 유의미성을 확보했습니다.
한편, 작년 FDA는 실사 결과 수탁 제조 회사에서 문제를 발견해 승인을 거부한 바 있지만, 올해 4월에 드디어 승인을 받게 되었습니다. Evaluate는 Anktiva가 2028년까지 8억 7,800만 달러의 매출을 기록할 것으로 예상했습니다.
9. Ensifentrine - 만성 폐쇄성 폐질환
▶ Company: Verona Pharma
▶ Indication: Chronic obstructive pulmonary disease (COPD)
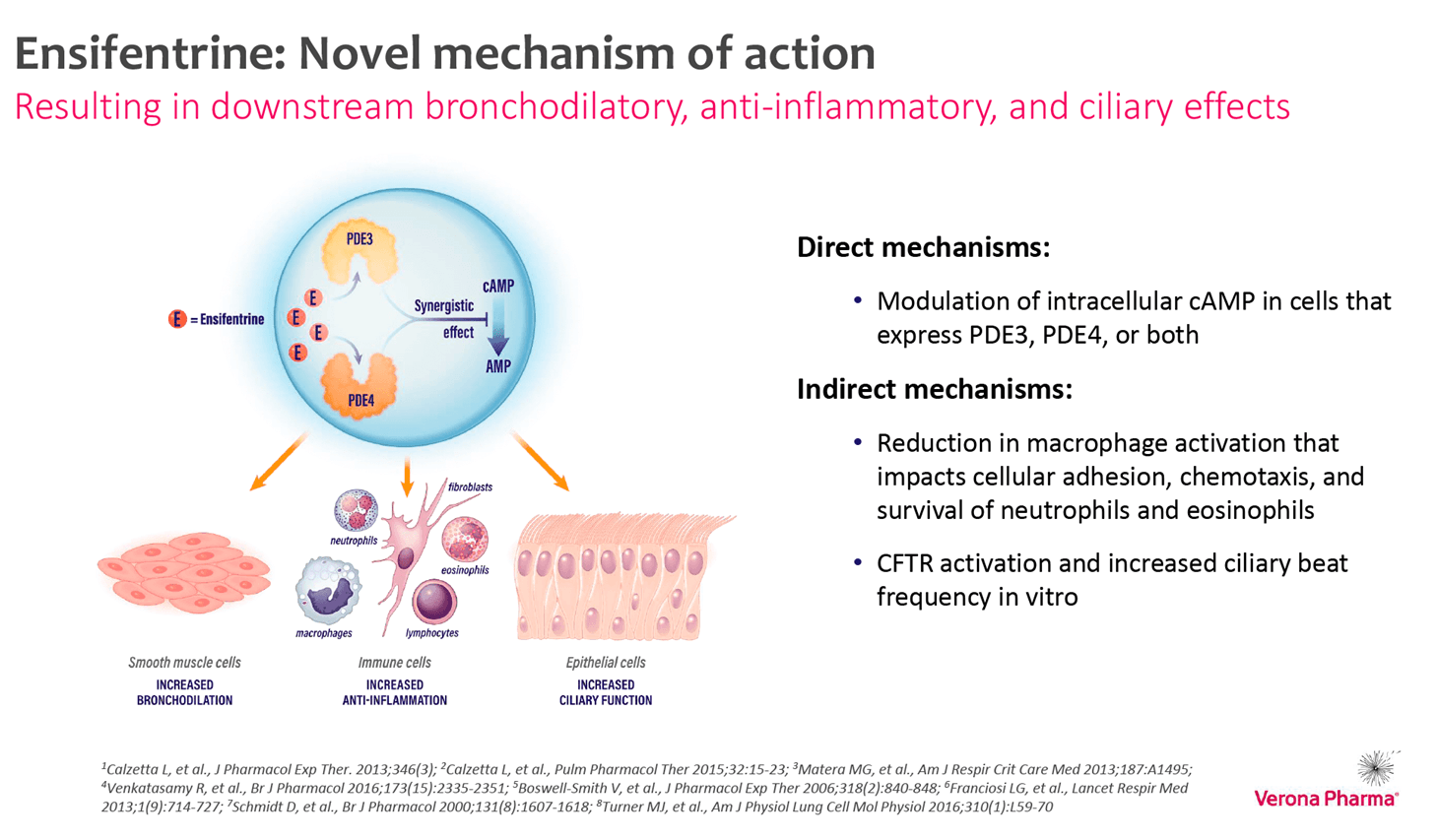
최초의 만성 폐쇄성 폐질환(COPD) 흡입형 치료제로 승인되었으며, 20년 만에 COPD 적응증으로 새롭게 출시되는 약입니다. 이 약물은 PDE3와 PDE4를 선택적으로 억제하는데, PDE3는 cAMP 분해를 억제해 평활근을 이완시키고 기관지를 확장합니다. 원래 PDE3는 심부전을 위한 약으로 개발되었으며, 이를 활용해 기관지 확장을 유도할 수 있게 되었습니다.
PDE4 억제는 대식세포의 활성화를 감소시키고, 염증성 사이토카인 생성을 줄여 염증 반응을 완화합니다. 뿐만 아니라, CFTR을 활성화하는데요, 이는 점액을 제거하는데 용이하도록 외부로 염화이온을 방출하는 메커니즘을 갖고 있습니다. 하지만 부작용으로는 요통, 고혈압 등이 보고된 바가 있습니다.
10. Imetelstat - 수혈 의존성 빈혈
▶ Company: Geron
▶ Indication: Lower risk myelodysplastic syndromes (MDS)
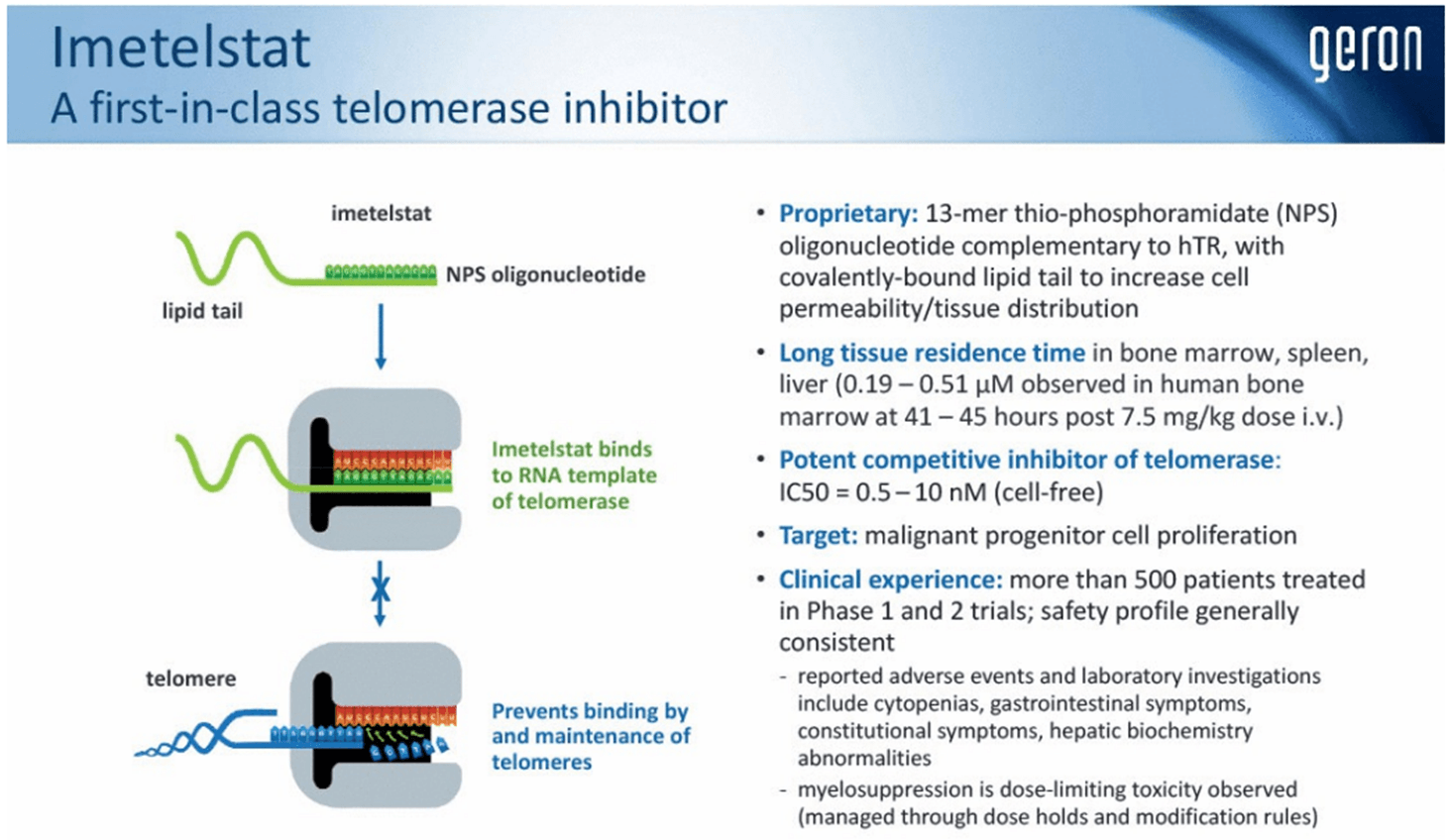
저위험 골수형성이상증후군(MDS) 환자의 수혈 의존성 빈혈 치료를 위한 최초의 텔로머레이스 억제제입니다. 이번 NDA 제출은 1차 평가변수인 8주 수혈 독립성(TI)이 위약 대비 유의하게 높았으며(p<0.001), IMerge 임상 3상 결과에서 이메텔스타트 8주 TI 반응자의 TI 기간 중앙값이 1년에 근접한 것을 기반으로 하고 있습니다. 이메텔스타트 치료 환자의 평균 헤모글로빈 수치는 위약 환자에 비해 시간이 지남에 따라 유의하게 증가해, 기존 적혈구 생성 자극제에 반응하지 않는 환자들에게 새로운 치료 옵션을 제공합니다.
이 약물의 기전은 telomerase 활성을 억제해 골수 악성 세포를 선택적으로 공격하는 것입니다. telomerase의 활성 부위에 결합해 텔로미어 합성을 막고, 이와 같은 원리로 텔로미어 길이를 줄여 암세포 분열을 억제하며 종양 성장을 차단합니다.
해당 약물을 개발한 회사 Geron은 저위험 MDS에서 초기 승인을 받은 후, 중등도-2 또는 고위험 골수섬유증으로 치료 범위를 확대할 계획입니다. JAK 억제제에 재발하거나 불응하는 골수섬유증 환자를 대상으로 한 3상 임상시험은 2025년 상반기에 중간 분석이 이루어질 예정이며, 최종 분석은 내년에 진행될 예정입니다. 이 임상시험은 2031년에 35억 달러의 가치가 있을 것으로 예상되는 또 다른 시장을 열 것으로 기대됩니다.
참고 문헌
In the Pipeline: Top Drug Candidates for FDA Approval in 2024 – Global X ETFs
Top 10 Most Anticipated Drug Launches Of 2024 | Biopharma PEG (biochempeg.com)